Las biopelículas son comunidades de microorganismos rodeados
de una matriz extracelular, que favorece la adhesión a las superficies, las cuáles
contribuyen a desarrollar una alta tolerancia a las moléculas con actividad
antimicrobiana, lo que significa que son difíciles de tratar con
antimicrobianos convencionales. Estas representan un riesgo para la salud, ya
que poseen altas tasas de morbilidad y mortalidad.
El origen
Las biopelículas fueron observadas por primera vez en el año 1684 por Anton Van Leeuwenhoek, cuando miró en el microscopio muestras de su boca, específicamente de la placa microbiana obtenida de sus dientes. Años más tarde, en 1864, Louis Pasteur describió dicho fenómeno en muestras alimenticias tomadas de las paredes de los barriles donde se almacenaba el vino.
Con el paso de los años el término biopelícula fue adquiriendo importancia e interés en el área de la salud. Se ha demostrado que las infecciones relacionadas con la formación de biopelículas son propensas a volverse crónicas y persistentes, a tener resistencia antimicrobiana, e incluso causar la muerte en ciertos pacientes.
¿Cómo se forman las biopelículas?
Las biopelículas están formadas por diferentes especies
microbianas como bacterias, hongos,
algas, entre otras; y se desarrollan en superficies que favorecen la
adherencia inicial de los microorganismos (porosas, ralladas o rugosas) o que carecen
de una correcta limpieza y desinfección. De este modo, en su mayoría son
consecuencia de higiene deficiente y su formación se puede resumir en los
siguientes pasos:
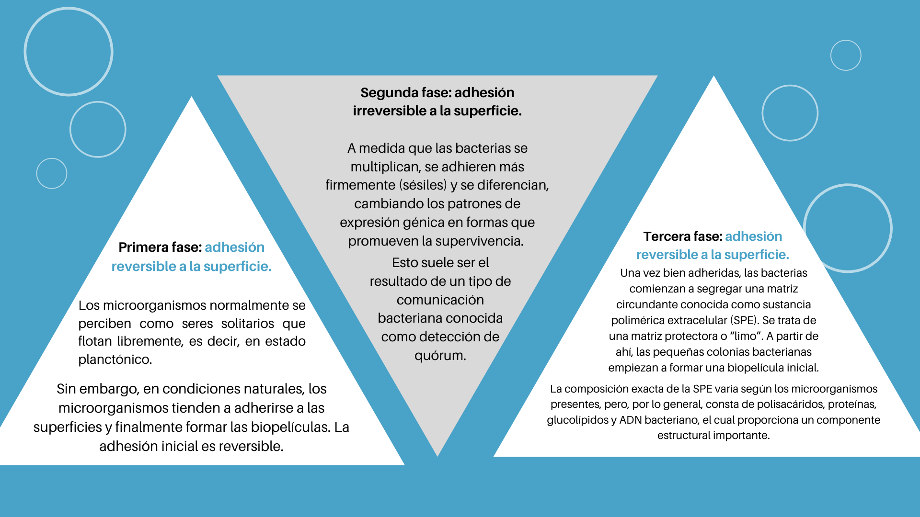
Varias proteínas y enzimas secretadas facilitan la adhesión firme de la biopelícula a la superficie. Las biopelículas maduras excretan continuamente bacterias planctónicas, microcolonias y fragmentos de biopelícula, que puede dispersarse y adherirse a otras partes de la superficie o bien a otras superficies, formando nuevas colonias de biopelícula.
De este modo, en vista de que viven en comunidades microbianas mixtas típicas de biopelículas, los microorganismos pueden compartir sus habilidades individuales para la supervivencia de todo el grupo. Por ello, tienen muchas ventajas de protección.
¿Cómo tardan en formarse?
Diversos estudios de laboratorio han demostrado que las bacterias planctónicas como los Estafilococos, Estreptococos y Pseudomonas, normalmente:
Se adhieren a la superficie luego de unos minutos.
Forman microcolonias fuertemente adheridas en un plazo de 2 a 4 horas.
Desarrollan la SPE inicial y presentan cada vez más resistencia a los biocidas en un plazo de 6 a 12 horas.
Evolucionan en colonias de biopelículas maduras extremadamente resistentes a los biocidas y excretan bacterias planctónicas en un plazo de 2–4 días (según las condiciones de crecimiento y las especies).
Se recuperan rápido de la interrupción mecánica y vuelven a formar biopelículas maduras en un plazo de 24 horas.
¿Qué ocasionan?
Las biopelículas son capaces de generar infecciones crónicas, persistentes, difíciles de erradicar debido a
que los microorganismos que crecen en ellas incrementan su tolerancia a las
moléculas con actividad antimicrobiana, y desarrollan mecanismos de resistencia
a los antibióticos. Además, la sustancia polimérica extracelular (SPE) ayuda a
evadir la respuesta inmunitaria del huésped.
¿Cuáles son las infecciones asociadas a biopelículas?
Se estima que aproximadamente el 65% de las infecciones bacterianas son causadas por bacterias creciendo en forma de biopelículas. Se distinguen dos tipos, las asociadas a dispositivos médicos y las asociadas a tejidos.
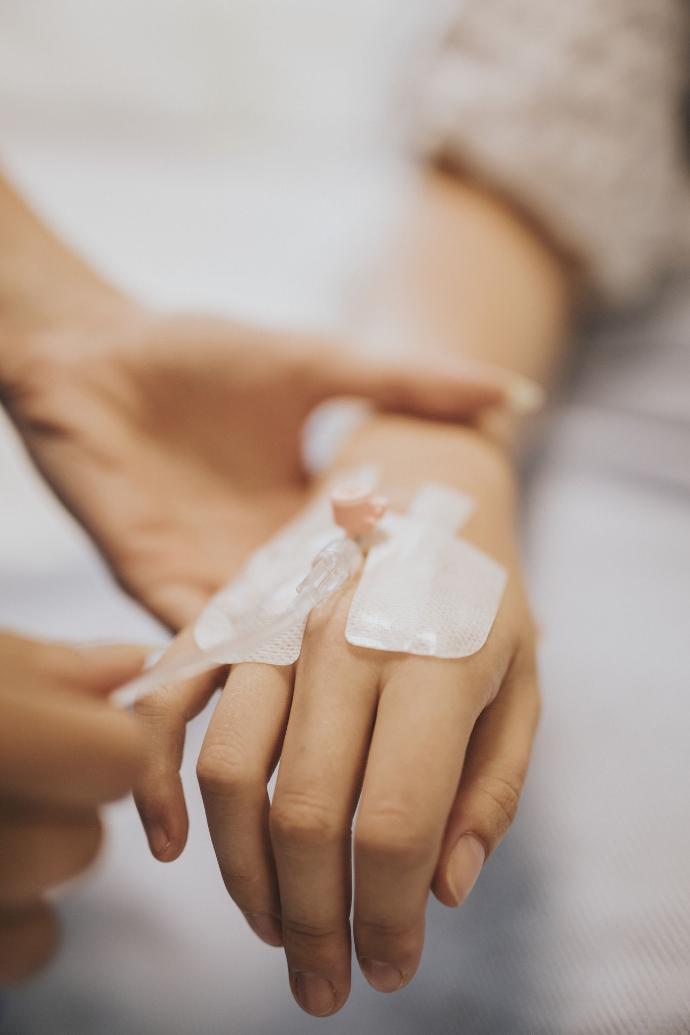
Infecciones en dispositivos médicos
Derivaciones ventriculares.
Lentes de contacto.
Catéteres centrales vasculares.
Válvulas cardiacas.
Marcapasos.
Injertos vasculares.
Implantes mamarios.
Tubos endotraqueales.
Catéteres urinarios.
Implantes ortopédicos.
Prótesis articulares.
Infecciones en tejidos
Otitis media crónica.
Sinusitis crónica.
Gingivitis.
Amigdalitis crónica.
Laringitis crónica.
Endocarditis.
Fibrosis quística.
Piedras renales
Infección del tracto biliar.
Infección del tracto urinario.
Osteomielitis.
¿Cómo afectan las biopelículas a las heridas?
La formación de biopelículas es muy común en las heridas,
sobre todo en las crónicas, donde del 60% a 100% de ellas las contienen en
alguna zona del lecho de la herida. Por otro lado, solo el 6% de las heridas
agudas se ven afectadas por la formación de biopelículas. Estas pueden retrasar
la cicatrización de las heridas y aumentar el riesgo de sobreinfección para el paciente, dado que estas contribuyen a
un estado inflamatorio crónico en un intento del cuerpo de eliminar la
biopelícula de la herida. De forma más específica, a medida que el cuerpo
intenta combatir las biopelículas a través de la respuesta inflamatoria, en
realidad le está proporcionando nutrición en forma de exudado, creando una
situación en la que el cuerpo combate ineficazmente las biopelículas, mientras genera daño en el tejido y retrasa la
cicatrización.
¿Cómo se identifican las biopelículas?
La forma más certera de identificarlas es a través de la de microscopia (fluorescencia, electrónica de barrido, confocal láser), que permiten observar directamente las biopelículas sobre biopsias de tejidos infectados o dispositivos médicos contaminados. Sin embargo, estas técnicas tienen costos muy elevados por lo que su aplicación dependerá de los recursos con los que se cuenten.
Existen otros métodos de laboratorio más accesibles con los que se puede sospechar la presencia de biopelículas, pero son mucho menos sensibles y específicos. Por lo tanto, se han propuesto características que permiten, a simple vista, sugerir el diagnóstico:

Por otro lado, es importante realizar la diferenciación entre
la biopelícula y el esfacelo, ya que estos suelen cohabitar en una herida
cronificada. La biopelícula estimula el ambiente inflamatorio incrementando
la permeabilidad vascular, incrementa el exudado y la aparición de esfacelo.
¿Cómo tratar las biopelículas en las heridas crónicas?
Una vez identificada la biopelícula, se presentan dos objetivos principales para el manejo y tratamiento:
Reducir la carga de la biopelícula
Mediante el desbridamiento mecánico de la herida, eliminando el tejido necrosado y contaminado.
Evitar que se reconstruya
Utilizando apósitos para tapar la herida y protegerla de una sobreinfección. También utilizando agentes antibacterianos en las curas, como la sulfadiazina de plata, pomadas antibióticas y soluciones antimicrobianas de amplio espectro como el polihexametileno biguanida (PHMB), ácido hipocloroso, ozonoterapia, entre otros.
¿Cuándo desaparece la biopelícula?
El indicador clínico más claro y evidente es la progresión de la cicatrización, junto con la reducción de la producción del exudado y esfacelo. Si se quiere saber de forma certera y definitiva entonces se deberá recurrir a las pruebas de laboratorio.
De acuerdo a la evolución y mejoría se procede a modificar el
tratamiento de las heridas. Según sea el caso se puede optar por reducir la
frecuencia de limpiezas y desbridamiento, e incluso evaluar nuevamente el uso
de los antimicrobianos tópicos.
Las practicas actuales reducen el riesgo de infección y cicatrización tardía. Aun así, los investigadores y profesionales de la salud, siguen trabajando en crear protocolos de acción que permitan mejorar el manejo de las biopelículas.
Natrox ha sido fundamental en muchos procesos de cicatrización de heridas crónicas, suministrando oxígeno continuo transdérmico y humidificado directamente al lecho de la herida, ayudando a la sanación total. Si deseas más información escríbenos a nuestro WhatsApp: 312 3290687